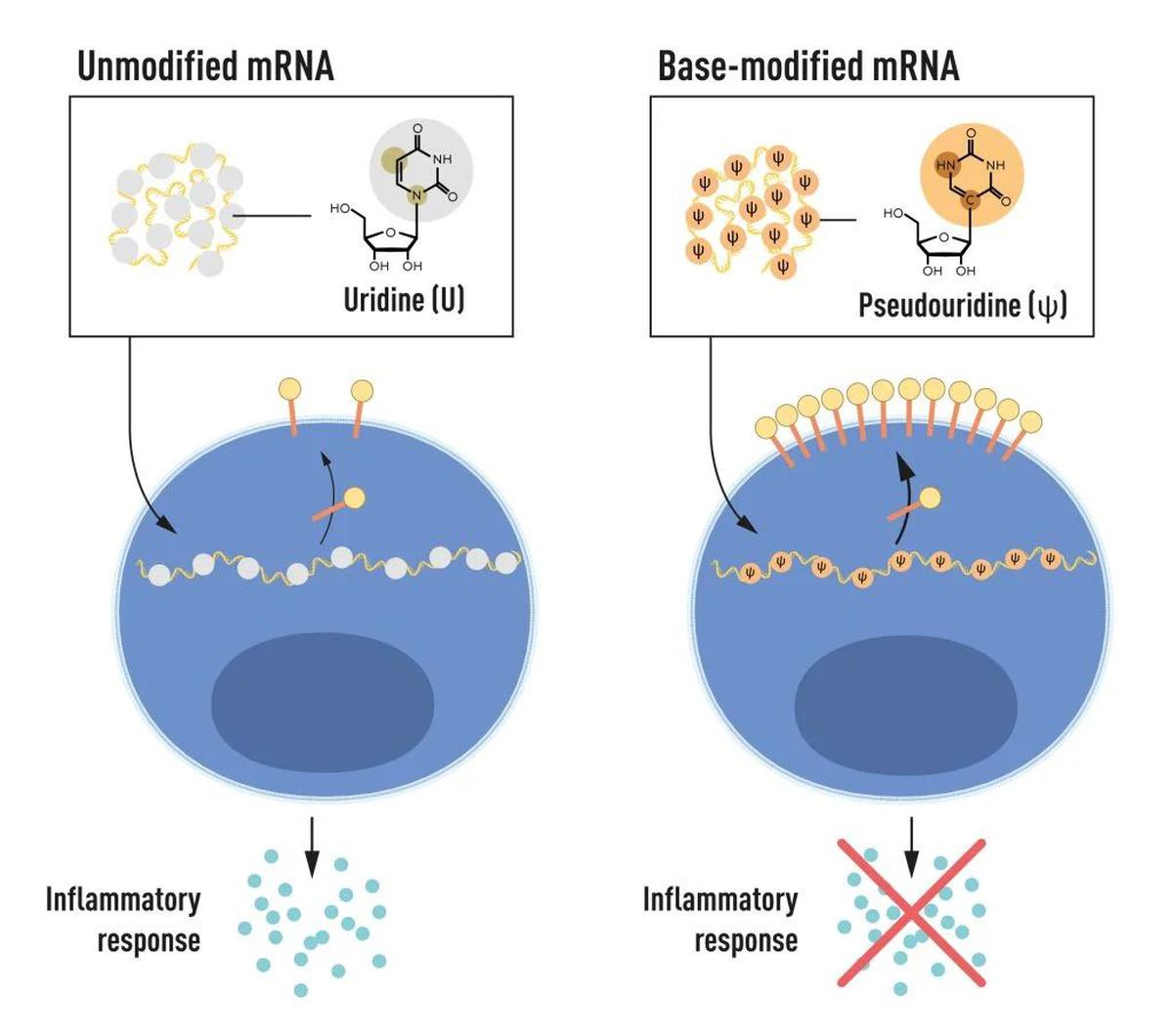
La historia tan lejana: El 2 de octubre comenzó la Semana de los Premios Nobel con la entrega del Premio de Fisiología y Medicina 2023 a Katalin Karikó y Drew Weissman. Recibieron el premio por sus “descubrimientos sobre modificaciones de bases de nucleósidos que permitieron el desarrollo de vacunas de ARNm eficaces contra el COVID-19”.
(Para conocer las principales noticias de salud del día, suscríbase a nuestro boletín informativo Health Matters)
¿Qué son las vacunas de ARNm?
El ARNm, que significa ARN mensajero, es una forma de ácido nucleico que transporta información genética. Al igual que otras vacunas, la vacuna de ARNm también intenta activar el sistema inmunológico para que produzca anticuerpos que ayuden a combatir la infección con un virus vivo. Sin embargo, mientras que la mayoría de las vacunas utilizan bacterias o virus debilitados o muertos para provocar una respuesta del sistema inmunológico, las vacunas de ARNm introducen sólo una parte del material genético que corresponde a una proteína viral. Suele ser una proteína que se encuentra en la membrana del virus llamada proteína de pico. Por lo tanto, la vacuna de ARNm no expone a las personas al virus en sí.
Redacción | Disparo en el brazo: sobre el Premio Nobel de Medicina 2023
Según un artículo de Thomas Schlake et al, en biología del ARN, el ARN como agente terapéutico se promovió por primera vez en 1989 después del desarrollo de una técnica de transfección in vitro ampliamente aplicable. Un par de años más tarde, se propuso el ARNm como plataforma de vacuna. Dice: “El ARNm ofrece grandes ventajas de seguridad. Al ser la construcción genética mínima, contiene sólo los elementos directamente necesarios para la expresión de la proteína codificada”. Un enfoque común de los fabricantes de vacunas durante la pandemia ha sido introducir una porción de la proteína de pico, el componente básico del coronavirus, como parte de una vacuna. Algunos fabricantes han envuelto el gen que codifica la proteína de pico en un virus inactivado que afecta a los chimpancés, llamado adenovirus de chimpancé. El objetivo es hacer que el cuerpo utilice su propia maquinaria para producir proteínas de pico a partir de un código genético determinado. El sistema inmunológico, cuando registre la proteína Spike, creará anticuerpos contra ella.
¿En qué se diferencian estas vacunas?
Un fragmento de ADN debe convertirse en ARN para que una célula produzca la proteína de pico. Aunque una vacuna de ARNm puede parecer un enfoque más directo para lograr que la célula produzca las proteínas necesarias, el ARNm es muy frágil y será destruido a temperatura ambiente o por las enzimas del cuerpo cuando se inyecta. Para preservar su integridad, el ARNm debe estar envuelto en una capa de lípidos aceitosos o células grasas. Una forma de pensar en esto es que una unidad de ARNm-lípido imita muy de cerca la forma en que un virus se presenta al cuerpo, excepto que no puede replicarse como tal. El ADN es mucho más estable y puede integrarse de forma más flexible en un vector de vacuna. En términos de rendimiento, ambos deberían ser igualmente efectivos.
Un desafío de las vacunas de ARNm es que deben congelarse entre -90 grados Celsius y -50 grados Celsius. Se pueden almacenar hasta dos semanas en congeladores comerciales y deben descongelarse a una temperatura de entre 2 y 8 grados centígrados, a la que pueden permanecer durante un mes. Pero una gran ventaja de las vacunas de ARNm y ADN es que, como solo requieren el código genético, es posible actualizar las vacunas a variantes emergentes y utilizarlas para una variedad de enfermedades.
Las vacunas de vectores virales, como Covishield, llevan ADN envuelto en otro virus, pero el ARNm es solo una hoja de instrucciones para producir proteínas de pico envueltas en un lípido (o molécula de grasa) para mantenerla estable. En el caso de la COVID-19, las vacunas de ARNm desarrolladas por Moderna, Pfizer y Gennova Biopharmaceuticals, con sede en Pune, estas instrucciones por sí solas son capaces de producir la proteína de pico, que luego el sistema inmunológico utiliza para preparar una defensa.
¿Por qué es esto significativo?
Después del anuncio del Premio Nobel, el Dr. Soumya Swaminathan, ex científico jefe de la OMS, publicó sobre el Premio Nobel al Dr. Karikó y al Dr. Weissman. «Veremos más productos basados en ARNm en un futuro próximo», afirmó. En su declaración, la Asamblea Nobel destacó que el entusiasmo por el desarrollo de la tecnología de ARNm con fines clínicos fue inicialmente limitado debido a obstáculos. “La idea de utilizar tecnologías de ARNm con fines terapéuticos y de vacunas despegó, pero surgieron obstáculos en el futuro. El ARNm transcrito in vitro se consideró inestable y difícil de administrar, lo que requirió el desarrollo de sistemas sofisticados de transporte de lípidos para encapsular el ARNm. Además, el ARNm producido in vitro dio lugar a reacciones inflamatorias».
¿Cuáles fueron los desafíos que tuvo que enfrentar el Dr. Karikó?
Las luchas del Dr. Karikó son particularmente notables entre los ganadores de este año. “Hace diez años… me echaron de Penn [Pennsylvania University] y obligada a jubilarse», le dijo a Adam Smith durante su entrevista con nobelprize.org después de que se anunciaran los ganadores. La Dra. Karikó ha pasado gran parte de su carrera al margen de los círculos académicos, siempre buscando subvenciones para financiar su investigación. Pasó la mayor parte de la década de 1990 escribiendo solicitudes de subvención para financiar su investigación sobre el ARNm. Creía que el ARNm era la clave para tratar enfermedades que necesitaban el tipo adecuado de proteína para resolver el problema.
Junto con el Dr. Weissman, publicó un artículo en 2005 destacando investigaciones innovadoras en este campo. En 2015, descubrieron cómo administrar ARNm a ratones utilizando una capa grasa llamada «nanopartículas lipídicas» que protegía el ARNm de la degradación. Ambas innovaciones fueron clave para el desarrollo de las vacunas COVID-19 desarrolladas por Pfizer y su socio alemán BioNTech.
(Con aportes de la agencia)
Este es un artículo Premium disponible exclusivamente para nuestros suscriptores. Leer más de 250 artículos premium de este tipo cada mes.
Has agotado tu límite de artículos gratuitos. Por favor apoye el periodismo de calidad.
Has agotado tu límite de artículos gratuitos. Por favor apoye el periodismo de calidad.
Tu has leído {{datos.cm.vistas}} afuera {{datos.cm.maxViews}} artículos gratis.
Este es tu último artículo gratuito.

«Apasionado experto en música. Gurú total del café. Amistoso adicto a los zombis. Especialista en cerveza. Experto en comida».
También te puede interesar
-
Video viral: pasajero enfurecido destruye computadoras en el aeropuerto. Le vendieron un billete falso de American Airlines.
-
Predator se hace pasar por un famoso YouTuber adolescente y chantajea a más de 280 niñas de todo el mundo para que realicen actos sexuales en una transmisión en vivo
-
Una foto de una mujer presumiendo durante una reunión con los talibanes en Afganistán recibe el visto bueno de Internet
-
Vuelo MH370 de Malaysia Airlines: una nueva teoría sugiere el lugar del avión 10 años después
-
Estudiantes indios protestan por los cambios en la política de inmigración canadiense por temor a la deportación